10月15日,罗氏宣布FDA批准Tecentriq(阿替利珠单抗)用于PD-L1阳性(PD-L1≥1%)早期非小细胞肺癌患者接受手术和含铂化疗后的辅助治疗。Tecentriq是一个获批用于NSCLC辅助治疗的免疫疗法。

罗氏医学官Levi Garraway表示:“Tecentriq作为一个用于NSCLC辅助治疗的免疫疗法,降低了早期肺癌患者的复发风险,增高了这类患者的治愈可能,开启了新纪元。”
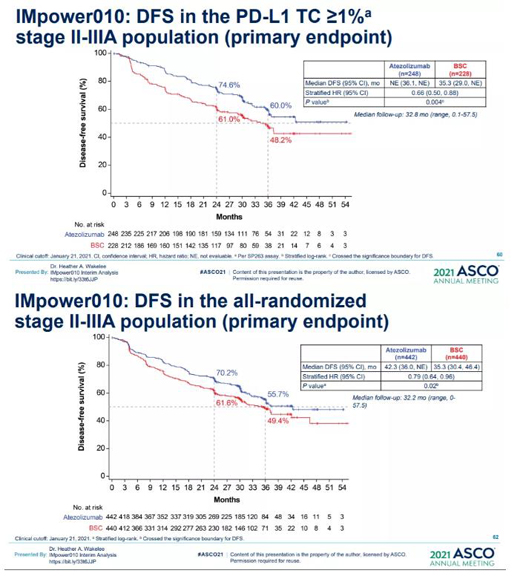
FDA此项批准主要基于III期IMpower010研究的中期分析结果。IMpower010研究采用随机、开放标签设计,在1005例接受手术和多4个周期含铂化疗的IB-IIIA期NSCLC患者中评估了Tecentriq 作为辅助疗法与较佳支持治疗(BSC)的疗效和安全性差异,多治疗16个周期。研究的主要终点是研究者评估的无病生存期(DFS),包括PD-L1阳性II-IIIA期亚组人群、全部随机入组的II-IIIA亚组人群、以及IB-IIIA期意向治疗患者人群。
结果显示,PD-L1表达阳性(PD-L1≥1%)II-IIIA期NSCLC患者接受Tecentriq辅助治疗,疾病复发或死亡风险相比BSC组低了34%(HR=0.66,95%CI: 0.50-0.88)。
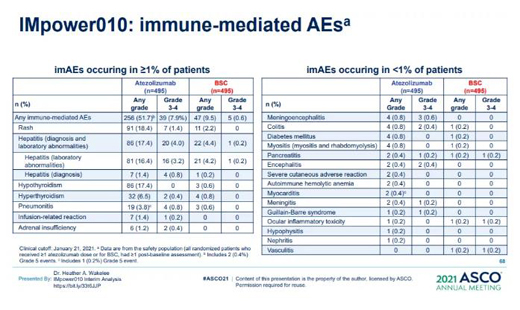
Tecentriq的安全性结果与之前的研究一致,未发现新的安全性事件。Tecentriq的致命和严重不良反应发生率分别为1.8%和18%。常见的严重不良反应包括肺炎(1.8%)、发热(1.2%)。
此项审批是在FDA的Orbis创新审批途径下完成。与FDA合作的国家药监机构,包括瑞士、英国、加拿大、巴西和澳大利亚,都对罗氏Tecentriq该适应症的上市申请进行了同步审评审批。
肺癌是全球癌症死亡原因,每年有 180 万人死于该疾病。肺癌患者中,85%-90%属于非小细胞肺癌。NSCLC按照疾病严重程度, 主要分为I~IV期。I期和II期都属于早期肺癌,癌细胞没有扩散,手术切除肺部肿瘤块、化疗、淋巴结清扫等方式是非常有效的治疗方案。I期肺癌的5年生存率可以达到70%-90%,II期肺癌的5年生存率可以达到50%-70%。大约50%的NSCLC患者在确实时处于早期(I 期和 II 期)或局部晚期(III 期)阶段。
早期肺癌患者的治疗目标是达到“治愈”,但是术后复发之后往往结局不佳。因此需要新的辅助治疗选择来尽可能地延长无病生存期,降低复发风险。Tecentriq此次获批成为十多年来早期NSCLC术后辅助治疗的一个重大突破。
声明:本文版权归原作者所有,转载文章仅为传播更多信息,如作者信息标记有误,或侵犯您的版权,请联系我们,我们将在及时修改或删除内容,联系邮箱:marketing@360worldcare.com


